코인피드
선행 읽기 추천 글:
현재 진행 중인 체지방 관리의 핵심 변수 3가지:
https://www.fmkorea.com/index.php?mid=best&sort_index=bookmark&document_srl=9722115116&listStyle=webzine
주의: 내용이 긴 글입니다
맨 아래 핵심 정리 참고
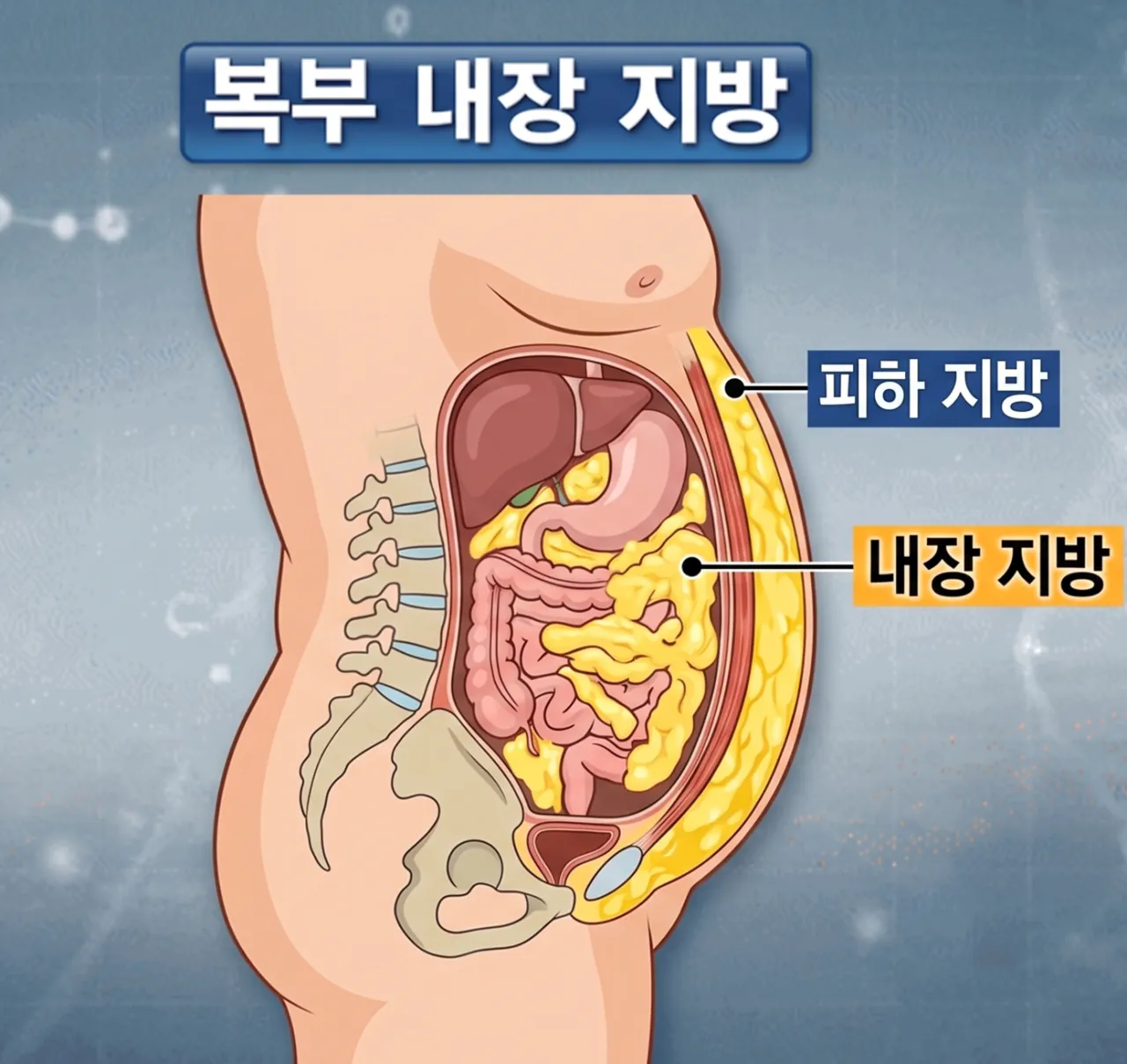
내장지방이 왜 건강을 위협하는가?
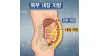
우리 몸의 지방은 크게 두 가지로 나뉜다
피부층 아래 축적되는 피하지방과 복강 내 장기 주변에 부착하는 내장지방
이 둘은 위치와 형태가 다를 뿐 아니라 신체에 끼치는 해로움도 전혀 다르다
피하지방은 단순히 에너지를 보관하는 저장고 역할만 한다
그러나 내장지방은 전혀 다른 작동 방식을 가지고 있다
내장지방은 간장 순환계라는 특수한 통로를 거쳐 간과 바로 연결되어 있다
그곳에서 배출되는 지방산과 염증성 물질들이 간으로 직접 유입된다
이렇게 되면 지방간, 인슐린 저항성, 대사증후군 같은 질환이 생긴다
결국 내장지방이 많다는 것은 단순한 체형 문제가 아니다
이는 우리 몸 내부에서 염증을 생산하는 시설이 계속 가동 중이라는 의미다
그런데 문제는 이 내장지방을 물리적으로 제거하기가 정말 어렵다는 것이다

마운자로에 CBL-514까지 함께 썼더니 내장지방이 단독 요법 대비 약 367% 추가 감소가 일어난 거임
약이 직접 닿지도 않은 내장지방이 이 정도로 줄어든 건 우연이 아니라, 피하지방이 사라지면서 몸의 지방 대사 방향 자체가 바뀐 결과임
약물 중단 후 요요현상도 55.9% → 25.2%로 절반 이하로 억제됐는데, 이게 가능한 이유가 CBL-514가 지방 세포의 수 자체를 줄여버리기 때문임
GLP-1 단독으로 사용할 경우 지방 세포 크기를 줄이지만 개수는 그대로 남아 있어서 약을 끊으면 다시 커지는데, CBL-514가 세포 수를 없애버리면 다시 찔 기반 자체가 줄어드는 거임
전략 2. 나노 약물로 내장지방에 직접 침투하기
우회 전략 말고 내장지방에 직접 파고드는 정면 돌파 연구도 있음
이게 나노의학 쪽 접근임
① 양이온성 나노물질 P-G3: 전하로 내장지방만 찾아가기
내장지방 표적 치료에서 가장 근본적인 문제가 뭐냐면 "어떻게 내장지방만 골라서 공략하냐" 는 거임
내장지방은 복강 안에 덩어리 형태로 여기저기 흩어져 있음
한 덩어리로 뭉쳐 있는 게 아니라 장간막, 대장 주변, 간 주변 등 각기 다른 위치에 나뉘어서 분포함
그래서 약을 혈관으로 넣었을 때 이걸 찾아가게 만드는 것 자체가 매우 어려운 문제였음
기존에는 어떻게 했냐면
특정 세포 표면 수용체를 인식하는 펩타이드 리간드를 나노입자에 붙여서
"이 수용체가 있는 곳으로 가라~"는 식의 능동 표적화 방식을 썼음
근데 이게 지방 조직에서는 생각보다 잘 안 됐음
지방 조직 환경이 복잡하고 수용체 발현이 일정하지 않아서 원하는 부위에 충분히 도달하기 전에 다른 곳에 흡수되거나 분해되는 경우가 많았음
그래서 컬럼비아 대학과 UNIST 연구진이 완전히 다른 방향으로 접근함
"수용체를 찾아가는 게 아니라, 전하 차이를 이용하자"
발견이 하나 있었음
비만으로 인해 비대해진 내장지방 조직은 세포 외 기질(ECM), 즉 세포들을 둘러싸고 있는 틀 안에 음전하를 띠는 분자들이 비정상적으로 많이 축적된다는 거임
이게 왜 생기냐면, 지방 세포가 과도하게 팽창하면서 ECM 구성 성분 중 헤파란 황산염이나 콘드로이틴 황산염 같은 음전하 당사슬 분자들이 과잉 발현되기 때문임
정상 지방 조직보다 비만 내장지방에서 이 음전하 밀도가 훨씬 높아짐
연구진은 이 특성을 역이용했음
강한 양전하를 띠는 나노입자를 만들면, 혈류를 타고 돌다가 내장지방의 음전하에 자석처럼 달라붙지 않겠냐는 발상임
이렇게 만든 게 P-G3 임
P-G3가 뭔지 구조부터 설명하면
PAMAM 덴드리머라는 물질이 있음
덴드리머는 나뭇가지처럼 사방으로 팔이 뻗어 있는 구조의 합성 나노분자인데, 표면에 아민기가 빽빽하게 달려 있어서 강한 양전하를 띰
이 중에서 generation 3, 즉 3세대 PAMAM이 P-G3임
크기도 작고 표면 양전하 밀도도 딱 적절한 수준이라 혈관 안에서 안정적으로 순환할 수 있음
여기에 콜레스테롤을 결합시킴
콜레스테롤은 기름과 친한 소수성 분자라서, 이걸 붙이면 나노입자가 지방 조직 환경에서 더 잘 흡착되고 세포 안으로 들어가기도 쉬워짐
결과적으로 P-G3는 "겉은 양전하로 내장지방을 찾아가고, 안은 지질 친화성으로 지방 세포 안에 잘 자리 잡는" 이중 구조를 갖게 됨
실제 작동 방식을 순서대로 보면 이럼
1단계: 혈류 순환
P-G3를 혈관에 주사하면 혈류를 타고 전신을 순환함
이때 정상 조직이나 다른 장기의 ECM은 음전하 밀도가 낮아서 P-G3가 강하게 달라붙지 않고 그냥 지나침
2단계: 내장지방 감지 및 흡착
비만 내장지방의 ECM에 도달하면 얘기가 달라짐
음전하 밀도가 비정상적으로 높은 이 환경에서 P-G3의 양전하와 강한 정전기적 인력이 형성되면서 나노입자가 흡착됨
특별한 수용체 없이도 전하 차이만으로 내장지방을 선택적으로 인식하는 거임
3단계: 내장지방 세포 내 작용
내장지방 조직에 유입된 P-G3는 비대해진 지방 세포가 지질을 추가로 더 저장하는 걸 억제함
동시에 비만 내장지방에서 만성적으로 진행되던 염증 반응을 완화하는 조직 리모델링을 수행함
이 방식이 신기한 건
수술도 아니고, 직접 주사도 아니고, 혈관으로 넣은 나노입자가 지 알아서 내장지방을 찾아가는 방식이라는 거임
기존 능동 표적화 방식이 수용체를 찾아가는 복잡한 구조였다면, 이건 전하 밀도라는 물리적 특성 하나만 이용하는 단순하면서도 강력한 수동 표적화임
내장지방이 비대할수록 음전하 밀도가 높아지니까, 오히려 더 심각하게 비만인 내장지방일수록 P-G3가 더 잘 달라붙는 아이러니한 자기 선택성도 갖고 있음
한 줄 요약하면
: 내장지방이 음전하를 띤다는 사실을 이용해서, 양전하 나노입자를 혈관에 넣으면 자석처럼 내장지방만 찾아가게 만든 뒤에
내장지방에 지질이 더 쌓이는 것을 막고 염증 반응을 완화하는 기술임
② PCL 나노입자 + 디설피람: 지방 세포 공장 자체를 없애기
이 기술을 이해하려면 먼저 질문 하나를 던져야 함
"지방을 없애는 것"과 "지방이 더 생기지 않게 막는 것" 중에 뭐가 더 근본적인 해결책이냐?
지금까지 대부분의 치료법은 전자, 즉 이미 있는 지방 세포를 없애는 데 집중했음
근데 이 연구는 후자를 파고들었음
"지방 세포가 새로 만들어지는 과정 자체를 차단하면 안 될까?"
이걸 이해하려면 지방 세포가 어떻게 생기는지부터 알아야 함
지방 세포는 처음부터 완성된 형태로 존재하는 게 아님
지방전구세포(Preadipocyte) 라는 미성숙 전구 세포가 먼저 있고, 이게 분화 과정을 거쳐 성숙한 지방 세포로 변함
성숙한 지방 세포는 내부에 거대한 지질 방울을 품고 있는 완전체 상태이고
전구세포는 아직 지질을 거의 안 품고 있는 예비 단계임
문제는 비만 상태에서 이 전구세포가 계속 분열하고 성숙한 지방 세포로 바뀌면서 지방 조직이 팽창한다는 거임
즉 전구세포는 지방 공장의 원자재임
이걸 없애면 공장이 돌아갈 수가 없는 구조임
그럼 어떤 약으로 이 전구세포를 없애냐
여기서 등장하는 게 디설피람(Disulfiram, DSF) 임
디설피람은 원래 알코올 의존증 치료제로 쓰이던 약임
알코올을 분해하는 효소를 억제해서, 술을 마시면 몸이 극도로 힘들어지게 만드는 방식으로 금주를 유도하는 약임
근데 이 약이 다른 기능도 있다는 게 밝혀졌음
몸의 대사 센서 역할을 하는 TRPA1 이온 채널을 활성화시켜서 지질이 세포 안에 축적되는 걸 줄이는 효과가 있음
인슐린 저항성 완화에도 영향을 주는 것으로 재조명받고 있음
근데 왜 지금까지 비만 치료제로 안 썼냐?
두 가지 문제가 있었음
첫째, 약 자체가 너무 불안정함
디설피람은 생리적 환경, 즉 혈액이나 체액 안에서 빠르게 분해돼버림
먹거나 주사해도 타겟 부위에 도달하기 전에 상당 부분이 사라짐
둘째, 뇌까지 퍼져버림
디설피람은 혈액-뇌 장벽을 쉽게 통과하는 특성이 있음
그래서 지방 조직만 건드리는 게 아니라 중추신경계까지 영향을 줄 수 있음
이 두 가지가 해결이 안 되니까 항비만 치료제로 직접 쓰기가 어려웠던 거임
이걸 해결하기 위해 나온 아이디어가 "나노입자 껍데기에 담아서 전달하자!"는 거임
여기서 쓰인 소재가 폴리카프로락톤(PCL) 임
PCL이 뭐냐면
수술용 봉합사나 의료용 이식재에도 쓰이는 생분해성 고분자 소재임
몸 안에서 서서히 분해되고 독성이 없어서 인체 적합성이 매우 높음
이 PCL로 나노입자 껍데기를 만들고 안에 디설피람을 넣으면
디설피람이 혈액 안에서 분해되지 않고 안전하게 보호된 채로 이동할 수 있음
만들어진 PCL-DSF 나노입자의 스펙을 보면
크기가 평균 203nm 정도임
이게 중요한 이유는 너무 크면 혈관 벽을 통과 못하고, 너무 작으면 신장에서 바로 걸러지기 때문에 이 사이즈가 혈류를 타고 안정적으로 돌아다니기에 최적의 범위임
제타 전위는 -20.7mV인데, 이 정도 음전하면 입자끼리 서로 밀어내서 뭉치지 않고 혈액 안에서 고르게 분산된 상태를 유지할 수 있음
약물 방출 방식도 잘 설계돼 있음
주사 후 30분 안에 약 11%가 먼저 방출되고
이후 96시간, 즉 4일에 걸쳐 나머지 91%가 서서히 방출됨
터뜨리듯 한꺼번에 나오는 게 아니라, 시간을 두고 천천히 흘러나오는 지속 방출 구조임
그래서 타겟 부위에서 약물 농도가 일정하게 유지됨
이제 진짜 핵심임
이 나노입자가 지방 세포의 발달 단계에 따라 완전히 다르게 행동한다는 거임
성숙한 지방 세포에 들어가면?
아무 일도 안 일어남
세포 생존율에 영향이 없음
대식세포에 들어가도 마찬가지임
근데 지방전구세포에 들어가면?
이야기가 완전히 달라짐
방출된 디설피람이 전구세포의 미토콘드리아를 직접 공격함
미토콘드리아가 왜 중요하냐면
세포의 에너지 발전소임
여기서 ATP라는 에너지를 만들어내는데, 이 과정이 유지되려면 미토콘드리아 내막에서 일정한 전위차, 즉 막 전위가 유지돼야 함
근데
1. 디설피람이 이 막 전위를 무너뜨려버림
2. 막 전위가 붕괴되면 미토콘드리아가 정상 작동을 멈추고, 동시에 내부에서 활성산소(ROS) 가 폭발적으로 만들어짐
3. 활성산소는 세포 입장에서 극도로 유해한 물질임
4. 이 상태까지 오면 세포는 자체적으로 사멸 명령을 내림
5. 그 경로가 카스파제 3/7 이라는 단백질을 절단하는 방식으로 작동하는데, 이게 활성화되면 세포는 깔끔하게 자멸사(Apoptosis) 로 사라짐
자멸사가 왜 중요하냐는 앞에서도 나왔지만 다시 짚으면
세포가 터지는 괴사는 내용물이 주변에 쏟아지면서 염증 반응을 폭발적으로 일으킴
자멸사는 세포가 스스로 포장된 채로 분해되면서 조용히 사라지는 과정이라 주변 조직에 염증을 거의 안 일으킴
이 기술의 진짜 의미가 뭐냐면
성숙한 지방 세포는 건드리지 않고, 새로운 지방 세포로 자라날 전구세포만 골라서 없애버린다는 거임
성숙한 지방 세포 → 안전
지방전구세포 → 자멸사 유도
이 선택성이 어디서 나오냐를 정확히 이해하려면 더 깊은 생화학 분석이 필요하지만, 현재로선 전구세포가 성숙한 지방 세포보다 미토콘드리아 대사에 훨씬 더 민감하게 반응하는 특성이 있기 때문으로 보고 있음
결과적으로 이 전략이 노리는 건
지방 세포를 지금 없애는 것보다
앞으로 지방 세포가 더 늘어날 수 없게 공장 가동 자체를 차단하는 것임
비만 상태에서 내장지방이 팽창하는 건 전구세포가 계속 성숙한 지방 세포로 분화하면서 숫자가 불어나는 과정인데, 그 분화의 원천인 전구세포를 제거하면 팽창 자체가 멈추는 구조임
한 줄 요약하면
: 알코올 치료제였던 디설피람을 나노입자 껍데기에 담아서, 지방 세포 공장의 원자재인 전구세포에만 선택적으로 미토콘드리아 폭탄을 투하해서 자멸사를 유도하는 기술임
③ MSNs-ATS + HAS: 프로히비틴 수용체 찾아가서 지방을 갈색지방으로 바꾸기
"지방 세포를 없애는 것"과 "지방 세포의 성질 자체를 바꾸는 것" 중에 뭐가 더 영리한 전략이냐?
앞에서 나온 P-G3는 지질 축적을 억제했고, PCL-DSF는 전구세포를 자멸사시켰음
근데 이 기술은 방향이 다름
이미 있는 지방 세포를 없애는 게 아니라, 그 세포의 기능 자체를 에너지 저장에서 에너지 소비로 전환시키는 것
이게 갈색지방화(Browning)라는 개념임
Q: 갈색지방이 뭐더라?
지방에는 크게 두 종류가 있음
백색 지방(White fat)
우리가 흔히 아는 지방임
에너지를 지질 형태로 저장하는 창고 역할을 함
운동 안 하거나 과식하면 쌓이는 게 이거임
내장지방도 기본적으로 백색 지방임
갈색 지방(Brown fat)
얘는 완전히 다름
에너지를 저장하는 게 아니라 열을 만들어서 에너지를 태우는 역할을 함
내부에 미토콘드리아가 엄청나게 많이 들어차 있고, UCP1이라는 단백질이 이 미토콘드리아에서 에너지를 ATP로 저장하는 대신 열로 방출시킴
쉽게 말하면 백색 지방은 배터리고, 갈색 지방은 발열체임
갓난아기들이 추위에서도 체온을 잘 유지하는 이유가 갈색 지방이 많기 때문이고, 성인이 되면서 점점 줄어듦
그럼 이 기술의 핵심적인 아이디어는 뭐냐
백색 내장지방을 갈색 지방처럼 바꿔버리면, 칼로리를 저장하는 대신 태우는 조직으로 변환된다
이게 Browning, 갈색지방화임
말이 쉽지..
문제는 어떻게 내장지방 세포 안에 이 신호를 정확하게 집어넣느냐임
여기서 등장하는 게 MSNs 임
메조다공성 실리카 나노입자라는 긴 이름인데, 구조가 독특함
실리카, 즉 이산화규소로 만든 나노입자인데 안이 벌집처럼 수천 개의 미세한 구멍으로 뚫려 있음
이 구조 덕분에 표면적이 극도로 넓어지고, 그 안에 약물을 엄청나게 많이 담을 수 있음
게다가 표면을 화학적으로 수식하기 쉬운 특성이 있어서, 원하는 리간드나 표적 분자를 표면에 붙이기가 용이함
즉 "약물을 많이 담을 수 있고, 표면에 GPS 역할을 하는 분자를 달기도 쉬운" 최적의 나노 플랫폼임
이 MSNs 표면에 붙인 GPS가 ATS 펩타이드임
ATS는 Adipose-Targeted Sequence의 약자고
CKGGRAKDC라는 9개의 아미노산으로 이루어진 짧은 펩타이드임
이게 왜 내장지방을 찾아가냐
백색 지방 조직의 혈관 내피 세포 표면에만 특이적으로 발현되는 수용체가 있음
바로 프로히비틴(Prohibitin) 이라는 단백질임
프로히비틴은 원래 세포 안에서 미토콘드리아 조립이나 유전자 발현 조절에 관여하는 단백질인데, 비만 상태의 백색 지방 혈관에서는 세포막 바깥쪽으로 노출되는 특이한 현상이 일어남
ATS 펩타이드는 이 프로히비틴에 강하게 결합하는 서열임
작동 방식을 순서대로 보면 이럼
1단계: 혈류 순환
MSNs-ATS를 혈관에 주사하면 혈류를 타고 전신을 돎
다른 장기 혈관 내피 세포에는 프로히비틴이 표면에 없으니까 그냥 지나침
2단계: 내장지방 혈관 내피 세포에 결합
백색 내장지방 조직의 혈관에 도달하면 ATS 펩타이드가 프로히비틴을 인식하고 달라붙음
3단계: 세포 안으로 진입
혈관 내피 세포가 이 나노입자를 삼키는 세포 내이입 과정을 통해 안으로 끌어들이고, 이를 통해 지방 세포 쪽으로 약물이 전달됨
이제 안에 담긴 약물인 HAS 가 작동함
HAS, 즉 Hydroxy-α-sanshool은 산초나무 열매에서 추출한 물질임
산초는 음식에 쓰이는 향신료인데, 먹으면 혀가 얼얼하고 저릿한 느낌이 드는 게 이 HAS 때문임
이게 단순한 맛 성분이 아니라 세포 수준에서 강력한 작용을 함
근데 이 물질도 디설피람처럼 생체 내에서 불안정함
혈액 안에서 산화되거나 구조가 변형되면서 약효를 잃기 쉬운 취약점이 있음
MSNs 껍데기가 이걸 보호하면서 내장지방 세포 안까지 안전하게 운반하는 거임
HAS가 내장지방 세포 안에 들어가면 TRPV1 이라는 수용체를 활성화함
TRPV1은 원래 열감각 수용체임
뜨거운 것이나 캡사이신, 즉 고추의 매운 성분에 반응하는 통증 수용체로 알려져 있음
근데 이 수용체가 지방 세포에도 있고, 활성화됐을 때 대사에 영향을 준다는 게 밝혀진 거임
HAS가 TRPV1을 활성화하면 두 가지 일이 일어남
첫째, 칼슘 이온이 세포 안으로 쏟아져 들어옴
TRPV1이 열리면서 이온 채널이 개방되고 세포 외부의 칼슘이 안으로 유입됨
이 칼슘 신호가 세포 안에서 연쇄 반응을 일으킴
둘째, PPAR-γ가 탈아세틸화됨
PPAR-γ는 지방 세포의 정체성을 결정하는 핵심 전사인자임
백색 지방 세포를 백색 지방 세포답게 유지시키는 마스터 스위치인데, 탈아세틸화가 일어나면 이 스위치의 작동 방식이 바뀜
백색 지방 유지 신호가 약해지고, 갈색 지방 특성을 발현하는 방향으로 전환이 시작됨
결과적으로 이 두 신호가 맞물리면서
에너지를 지질로 저장만 하던 백색 내장지방 세포가
열을 만들고 에너지를 태우는 갈색 지방 특성을 가진 세포로 변환됨
세포가 없어지는 게 아니라 성질이 바뀌는 거임
동물 실험에서 HAS를 그냥 단독으로 투여했을 때보다 MSNs-ATS에 담아서 투여했을 때 항비만 효과와 내장지방 표적 선택성이 명확히 더 높게 나왔음
나노입자가 없으면 HAS가 혈액에서 분해되거나 엉뚱한 곳에 퍼지는데, 나노입자가 이걸 보호해서 내장지방까지 제대로 데려다 놓는 역할을 하는 거임
여기서 한 단계 더 나아간 기술이 FOSSIL 임
FOSSIL은 포스콜린이라는 물질을 탑재한 지질-실리카 나노 하이브리드 입자임
포스콜린은 식물에서 추출한 물질로, 세포 안에서 cAMP라는 신호 분자를 늘려서 대사 활성화를 유도하는 효과가 있음
이걸 FOSSIL 나노입자에 담아서 성숙한 인간 지방 세포에 적용했더니 숫자들이 학계를 뒤집어 놓을 수준으로 나왔음
UCP1이 400배 과발현됨
UCP1이 뭔지 다시 정리하면
미토콘드리아 내막에 있는 단백질인데, 에너지 생산 과정을 중간에 끊어서 ATP 대신 열로 방출시키는 역할을 함
갈색 지방의 핵심 특성이 바로 이 UCP1이 많다는 거임
이게 400배가 올라간다는 건 지방 세포가 갑자기 강력한 발열 모드로 전환된다는 뜻임
Cox7A1도 80배 과발현됨
이것도 미토콘드리아 에너지 대사에 관여하는 단백질임
이게 같이 올라가면 지방 세포의 전체적인 에너지 연소 능력이 폭발적으로 증가함
아디포넥틴이 6000배 이상 증가함
아디포넥틴은 지방 세포에서 분비되는 호르몬인데, 인슐린 민감성을 높이고 염증을 억제하는 유익한 호르몬임
비만할수록 이 수치가 낮아지는 게 일반적인데, 6000배 이상 올라간다는 건 대사 환경 전체가 뒤집히는 수준임
전신 인슐린 민감성이 극적으로 개선되면서 당뇨 관련 지표까지 같이 좋아지는 방향으로 이어짐
정리하면 MSNs 계열 기술의 전략은 이럼
한 줄 요약하면
: 백색 내장지방 혈관에만 있는 프로히비틴 수용체를 GPS 삼아 나노입자가 정확히 찾아가고, 안에 담긴 HAS가 지방 세포 안에서 TRPV1을 건드려서 에너지 저장 창고를 에너지 소비 발열체로 전환시키는 기술임
전략 3. 빛으로 내장지방을 태우기: 광역학 치료와 광열 치료
지금까지 나온 전략들을 정리하면
P-G3는 전하로 내장지방을 찾아가서 지질 축적을 억제했고
PCL-DSF는 나노입자로 전구세포를 자멸사시켰고
MSNs-ATS는 수용체를 GPS 삼아 찾아가서 지방을 갈색지방으로 바꿨음
이 모든 기술의 공통점은 약물이 혈류를 타고 돌아다니면서 표적을 찾는 방식임
여기서 한 단계 더 나아간 개념이 등장함
약물이 표적에 도달했다고 해서 바로 작동하는 게 아니라, 외부에서 빛을 쏴줘야만 활성화되는 방식
이게 광역학 치료(PDT)와 광열 치료(PTT)임
기본 개념부터 설명하면
감광제라는 물질이 있음
평소에는 완전히 무해하고 아무 작용도 안 함
근데 특정 파장의 빛을 받으면 갑자기 반응을 일으킴
작동 방식은 이럼
1단계: 감광제를 혈관에 주사
2단계: 감광제가 혈류를 타고 돌다가 표적 조직에 축적될 때까지 기다림
3단계: 외부에서 레이저나 특정 파장의 빛을 쏨
4단계: 빛을 받은 감광제가 활성화되면서 주변 세포를 파괴하거나 대사를 변환시킴
이 방식의 장점은 "빛이 닿는 곳에서만 반응이 일어난다" 는 거임
감광제가 다른 조직에 있어도 빛을 안 쏘면 아무 일도 안 생김
시간과 공간을 동시에 제어할 수 있는 정밀 치료임
3.1. AIEgens: 산소 없이도 내장지방을 터뜨리는 감광제
광역학 치료가 기존에 안고 있던 결정적인 문제가 하나 있었음
비만 내장지방에서는 기존 감광제가 제대로 작동을 못했음
왜 그런지 이해하려면 기존 감광제가 어떻게 작동하는지부터 알아야 함
기존 감광제, 대표적으로 Ce6 같은 물질은
빛을 받으면 산소 분자에 에너지를 전달해서
단일항 산소(Singlet oxygen) 라는 고반응성 산소 분자를 만들어냄
이 단일항 산소가 주변 세포를 공격해서 파괴하는 방식임
이걸 Type II 광역학 반응이라고 함
근데 비만 환자의 내장지방에는 치명적인 문제가 있음
1. 지방 세포가 과도하게 비대해지면 세포들이 빽빽하게 밀집됨
2. 그러면 지방 조직 안으로 혈관이 충분히 들어오지 못함
3. 혈관이 부족하다는 건 산소 공급이 부족하다는 뜻임
= 결과적으로 비만 내장지방은 만성적인 저산소 상태에 놓여 있음
여기서 기존 Type II 감광제를 쓰면 어떻게 되냐
반응에 필요한 산소 자체가 없으니까 단일항 산소를 못 만들고
감광제가 있어도, 빛을 쏴도 아무 반응이 안 일어남
이 문제를 완전히 다른 방식으로 해결한 물질이 TTMN과 MeTTMN 임
이 물질들은 AIEgens 계열임
AIE는 Aggregation-Induced Emission의 약자로
분자가 뭉칠수록 오히려 발광 효율이 높아지는 특이한 성질을 가진 물질들을 말함
일반적인 형광 물질은 분자가 뭉치면 서로 소광시켜서 빛을 못 내는데, AIEgens는 반대로 뭉칠수록 더 강하게 발광함
왜 이게 내장지방에서 유리하냐?
TTMN과 MeTTMN은 소수성 물질, 즉 물을 싫어하고 기름을 좋아하는 성질임
혈액은 수성 환경이라서 이 물질들은 혈액 안에서 자연스럽게 뭉쳐서 돌아다님
그러다가 지방 세포 안의 지질 방울(Lipid droplet) 을 만나면 강하게 파고들어 안에 농축됨
지질 방울은 지방 세포가 트리글리세라이드를 저장하는 거대한 기름 덩어리임
비만 지방 세포일수록 이 지질 방울이 크고 양도 많음
TTMN은 여기 안으로 들어가서 뭉친 상태가 되고, AIEgens 특성상 이 상태에서 발광 효율이 최고치에 달함
이제 빛을 쏘면 어떻게 되냐
기존 감광제와 달리 TTMN은 산소가 필요 없음
빛을 받으면 주변의 산소 분자가 아니라 지질 방울 안의 생체 분자와 직접 전자를 교환함
이걸 Type I 광역학 반응이라고 함
이 과정에서 두 가지 극도로 반응성이 높은 물질이 만들어짐
하이드록실 라디칼(•OH) 과 초과산화물(•O2⁻)
이 자유 라디칼들이 지질 방울 내부에서 연쇄 반응을 일으킴
연쇄 반응의 흐름을 보면
자유 라디칼이 지질 분자의 전자를 빼앗음
→ 전자를 빼앗긴 지질 분자가 불안정해지면서 라디칼로 변함
→ 이 라디칼이 옆 지질 분자의 전자를 빼앗음
→ 또 라디칼이 생김
→ 이 과정이 끝없이 반복됨
이게 지질 과산화(Lipid peroxidation) 임
지질 방울 안의 지질 분자들이 도미노처럼 연쇄적으로 산화되면서 전부 망가지는 거임
지질 방울이 이렇게 과산화물로 가득 차버리면
세포는 내부에서 회복 불가능한 손상을 감지하고
페롭토시스 유사 자멸사라는 경로로 사멸함
페롭토시스는 원래 철 의존성 세포 사멸 경로인데, 지질 과산화가 한계를 넘어설 때 일어나는 세포 사멸 방식임
괴사처럼 터지는 게 아니라 자멸사 계열이라서 주변 염증 반응이 상대적으로 적음
이 기술의 안전성이 뛰어난 이유가 따로 있음
지질 방울이 없는 세포에는 반응이 안 일어남
TTMN이 농축되려면 지질 방울이 있어야 함
지질 방울이 작거나 없는 전구세포, 근육 세포, 피부 세포에는 TTMN이 농축이 안 됨
농축이 안 되면 빛을 쏴도 자유 라디칼이 거의 생성되지 않음
즉 지질 방울이 클수록, 즉 더 비대한 지방 세포일수록 더 강하게 타격을 받는 자기 선택적 파괴임
동물 실험에서 내장지방이 65% 이상 감소하는 결과가 나왔음
But, 한 가지 현실적인 문제가 있음
빛이 복강 깊숙한 내장지방까지 닿을 수 있냐는 거임
피부 위에서 레이저를 쏘면 피부와 근육층을 통과해야 해서 에너지가 많이 소실될 수밖에 없음
그래서 이 기술은 복강경 광섬유 기술과 결합하는 방향으로 발전하고 있음
복강경으로 광섬유를 배 안으로 직접 집어넣어서 내장지방 바로 옆에서 레이저를 쏘는 방식임
절개 없이 작은 구멍만 내면 되는 최소 침습 방식이라 기존 수술보다 훨씬 안전함
3.2. 광열 치료: 빛을 열로 바꿔서 지방을 태우기
광역학이 빛으로 자유 라디칼을 만들어 세포를 파괴하는 방식이라면
광열 치료는 방향이 다름
빛 에너지를 열에너지로 변환해서 지방 세포를 열로 공격하거나 대사 변화를 유도하는 방식임
여기서 쓰이는 게 금 나노스타(Gold nanostars) 와 구리 나노닷(CuS-NDs) 같은 무기 나노물질임
이 금속 나노물질들은 독특한 광학적 특성이 있음
표면 플라즈몬 공명(Surface Plasmon Resonance) 이라는 현상 때문에, 특정 파장의 빛을 쏘면 나노입자 표면의 자유 전자들이 공명을 일으키면서 빛 에너지를 극도로 효율적으로 흡수함
흡수된 에너지가 열로 변환되면서 나노입자 주변 온도가 급격하게 올라감
레이저를 쏘는 동안 나노입자 주변 온도가 국소적으로 수십 도씩 올라갈 수 있음
이 열이 내장지방에서 두 가지 방향으로 작용함
첫째, 직접 지방 세포를 파괴함
임계 온도 이상이 되면 지방 세포가 물리적으로 손상됨
둘째, 더 흥미로운 작용: 갈색지방화 유도
국소 온도가 올라가면 HSF1(열충격 인자 1) 이라는 신호 단백질이 활성화됨
HSF1은 세포가 열 스트레스를 받을 때 작동하는 생존 신호인데, 이게 지방 조직에서 활성화되면 UCP1 발현을 증가시킴
UCP1이 올라간다는 건 앞에서 설명했듯이 에너지를 태우는 갈색지방 특성이 켜지는 거임
열로 일부 세포를 파괴하면서 동시에 남은 세포들을 에너지 소비 모드로 전환시키는 이중 효과임
치료가 끝난 후에도 갈색지방화된 세포들이 계속 에너지를 소비하는 환경이 유지됨
한편 광역학과 광열을 결합한 융합 전략도 나오고 있음
Ce6라는 감광제에 올레산(Oleic acid, OA) 리간드를 붙인 복합체가 대표적임
올레산은 내장지방 세포의 GPR119라는 수용체를 인식하는 리간드임
즉 이 복합체는 GPR119가 있는 내장지방을 찾아가는 GPS를 달고 있는 거임
내장지방에 도달한 뒤 빛을 쏘면
AMPK 경로가 활성화됨
AMPK는 세포의 에너지 센서로 에너지가 부족할 때 켜지는 스위치인데, 이게 활성화되면 지방 분해가 촉진되고 포도당 흡수가 증가함
동시에 염증성 사이토카인이 극도로 억제됨
내장지방이 만들어내는 만성 염증 신호가 차단되면서 당뇨병성 내분비 환경 자체가 리모델링되는 결과로 이어짐
단순히 지방을 없애는 게 아니라 내장지방이 만들어내던 대사 교란 신호까지 같이 차단하는 거임
한 줄 요약하면
: 감광제를 내장지방에 쌓이게 한 뒤 외부에서 빛을 쏘는 방식으로, 산소 없이도 자유 라디칼로 지방 세포를 파괴하거나 열로 갈색지방화를 유도하는 시공간적 정밀 치료임
전략 4. FAT-ATTAC: 지방 세포만 골라서 죽이면 몸이 어떻게 반응하나
지금까지 나온 기술들은 전부 "어떻게 내장지방을 없애냐" 에 집중했음
근데 과학자들 입장에서 그것보다 더 근본적인 질문이 하나 있었음
"지방 세포를 선택적으로 없앴을 때 몸이 어떻게 반응하는지 우리가 실제로 알고 있냐"
이게 왜 중요한 질문이냐?
내장지방을 파괴하면 안에 있던 지질 덩어리와 세포 잔해가 쏟아져 나옴
이게 면역계를 자극할 수도 있고, 대사 시스템에 예상치 못한 충격을 줄 수도 있음
더 심각한 염증을 유발할 수도 있고, 반대로 괜찮을 수도 있음
근데 이걸 인체에서 직접 실험하는 건 불가능함
사람한테 "지방 세포만 골라서 전부 죽여볼게요"라고 할 수는 없으니까
이 질문에 답하기 위해 만들어진 게 FAT-ATTAC 마우스 모델임
FAT-ATTAC은 Fat Apoptosis Through Targeted Activation of Caspase-8 의 약자임
한국어로 풀면 "카스파제-8의 표적 활성화를 통한 지방 자멸사" 임
4.1. 어떻게 지방 세포만 골라서 죽이냐
이걸 이해하려면 먼저 카스파제(Caspase) 가 뭔지 알아야 함
카스파제는 세포 안에 있는 효소인데, 세포 자멸사를 실행하는 분자 가위 역할을 함
평소에는 비활성 상태로 잠들어 있다가, 자멸사 신호가 오면 활성화되면서 세포 사멸 과정을 실행함
그 중에서 Caspase-8은 자멸사 신호 전달 경로의 초반부에서 작동하는 핵심 스위치임
이게 켜지면 아래 단계 카스파제들이 연쇄적으로 활성화되면서 세포 사멸이 시작됨
FAT-ATTAC 마우스는 유전자 조작으로 특수 융합 단백질이 삽입돼 있음
이 융합 단백질은 두 부분으로 구성됨
Caspase-8 + FKBP (FK506 결합 단백질)
이 융합 단백질이 발현되는 곳이 핵심임
오직 성숙한 지방 세포의 세포막에서만 발현됨
전구세포도 아니고, 근육 세포도 아니고, 간 세포도 아님
성숙한 지방 세포에서만 이 단백질이 만들어짐
평상시에 이 마우스는 그냥 일반 마우스임
정상적으로 지방 조직을 형성하고 대사 기능을 수행함
융합 단백질은 있지만 활성화가 안 된 상태라서 아무 일도 안 일어남
여기에 AP20187 이라는 화학 물질을 주사하는 순간 상황이 달라짐
AP20187은 Dimerizer라고 부르는 물질임
이 물질이 하는 일이 딱 하나임
FKBP 두 개를 강제로 연결시키는 것
작동 순서를 보면
1단계: AP20187이 혈류를 타고 지방 세포막에 도달함
2단계: 세포막에 있는 FKBP 융합 단백질 두 개를 AP20187이 양쪽에서 잡아서 강제로 붙여버림
3단계: 두 단백질이 밀착되면서 Caspase-8이 서로를 활성화시킴. 잠들어 있던 procaspase-8이 절단되면서 활성 형태로 전환됨
4단계: 활성화된 Caspase-8이 하위 카스파제들을 연쇄적으로 작동시키면서 자멸사 명령이 실행됨
5단계: 오직 지방 세포에서만 이 과정이 일어나기 때문에 지방 세포만 선택적으로 자멸사함
결과가 어느 정도였냐
AP20187 주사 후 단 2주 만에
CT 촬영에서 복강과 피하에 있던 지방 저장소가 흔적도 없이 사라짐
이걸 인위적 지방위축증이라고 부름
지방이 병적으로 없어지는 상태인데, 이 경우엔 인위적으로 만들어낸 거임
이제 진짜 질문이 나옴
지방 세포가 이렇게 대규모로 사라지면 몸은 어떻게 반응하냐?
4.2. 괴사 vs 자멸사: 면역계가 완전히 다르게 반응함
이걸 이해하려면 비만 상태에서 지방 세포가 자연적으로 죽을 때 어떤 일이 벌어지는지부터 봐야 함
비만 상태에서의 자연적 세포 죽음: 괴사(Necrosis)
비만이 심해지면 지방 세포가 한계 이상으로 팽창함
지나치게 비대해진 세포는 산소와 영양 공급이 부족해지면서 결국 질식해서 죽음
이때 일어나는 게 괴사(Necrosis) 임
괴사는 세포가 그냥 터져버리는 거임
내부 내용물이 밖으로 전부 쏟아져 나옴
이게 주변 조직 입장에서는 엄청난 독성 자극임
이 잔해를 감지한 면역 세포들이 달려옴
달려오는 건 M1 대식세포임
M1 대식세포는 염증을 일으키는 공격형 면역 세포임
이들이 죽은 지방 세포 주변에 모여서 크라운 유사 구조(Crown-like structures, CLS) 라는 염증 집합체를 형성함
비만 환자 지방 조직을 현미경으로 보면 이 구조가 보임
죽은 지방 세포를 면역 세포들이 왕관 모양으로 둘러싸고 있는 형태임
여기서 끝나지 않음
M1 대식세포 안에 있는 NLRP3 인플라마좀이 활성화됨
인플라마좀은 면역계의 비상 경보 시스템 같은 거임
NLRP3가 켜지면 ASC와 Caspase-1 단백질이 동원되고
IL-1β와 IL-18 이라는 강력한 염증성 사이토카인이 대량으로 방출됨
이 사이토카인들이 혈류를 타고 전신으로 퍼지면서
인슐린 수용체 신호를 방해하고 전신 인슐린 저항성을 악화시킴
즉 비만 → 지방 세포 괴사 → 염증 폭발 → 인슐린 저항성 악화 → 당뇨로 이어지는 악순환의 분자적 정체가 이거임
FAT-ATTAC에서 유도된 죽음: 자멸사(Apoptosis)
반면 FAT-ATTAC 모델에서 Dimerizer로 유도된 지방 세포 사멸은 완전히 다른 양상을 보임
자멸사는 세포가 스스로 정리하면서 사라지는 과정임
세포가 터지는 게 아니라 내부에서 체계적으로 분해되면서 소포체로 포장된 채 조각남
이 포장된 조각들을 세포 잔해라고 하는데, 주변 조직에 독성 물질을 흘리지 않음
면역계가 이 상황을 어떻게 감지하냐
달려오는 대식세포의 종류가 다름
괴사에는 염증성 M1 대식세포가 오는데
자멸사에는 M2 대식세포가 대거 유입됨
M2는 M1의 반대임
염증을 일으키는 게 아니라 항염증 작용을 하면서 조직을 수복하는 청소부형 면역 세포임
죽은 세포 잔해를 깔끔하게 탐식해서 처리하고 조직 회복을 돕는 역할을 함
분자 수준에서 측정한 결과를 보면 차이가 더 명확함
염증의 핵심 지표인 NLRP3, ASC, Caspase-1, TXNIP 같은 인플라마좀 단백질이
자멸사가 일어나는 동안 전혀 관찰되지 않음
오히려 반대로 MCP-1이나 MMP12 같은 조직 회복 관련 유전자들이 대거 상향 조절됨
전신 염증 수치도 억제된 상태로 유지됨
한 가지 더 놀라운 발견이 있었음
Dimerizer 투여를 중단하면 지방이 다시 자라남
지방 세포가 전부 사라진 상태에서 약물을 끊으면
전구세포들이 다시 분화해서 새롭고 건강한 지방 세포가 재생됨
완벽한 가역성이 증명된 거임
지방을 없애되, 필요하면 다시 돌아올 수 있는 거임
이 모델이 내장지방 치료 연구 전체에 던진 메시지가 뭐냐
CBL-514든 나노 의학이든 광역학 치료든
이 기술들이 공통적으로 추구하는 게 자멸사 유도임
그게 왜 옳은 방향인지를 FAT-ATTAC이 분자 수준에서 증명해준 거임
지방 세포를 없애는 것 자체가 문제가 아님
어떻게 없애냐가 전부임
터뜨려서 없애면 염증 폭탄이 되고
자멸사로 없애면 오히려 만성 염증이 역전되면서 조직이 재건됨
비만의 핵심 병리가 만성 염증과 인슐린 저항성인데, 자멸사 유도 방식이 이 두 가지를 동시에 해결하는 방향임을 증명한 거임
한 줄 요약하면
: 유전자 조작 마우스에서 지방 세포만 골라 자멸사시켰더니 염증이 터지는 게 아니라 오히려 조직이 회복되는 방향으로 진행됐고, 이게 자멸사 기반 내장지방 표적 치료 전략 전체의 과학적 근거가 됨
전략 5. 칼 한 번 안 대고 내장지방을 녹이는 기술들
지금까지 나온 전략들을 다시 정리하면
약물을 혈류에 태워서 내장지방을 찾아가게 하거나
빛을 이용해서 지방 세포를 파괴하는 방식이었음
이 방식들의 공통점은 뭔가를 몸 안에 넣어야 한다는 거임
나노입자든 감광제든 약물이든 체내에 투여하는 과정이 필요함
여기서 완전히 다른 방향의 연구가 등장함
아무것도 넣지 않고, 외부에서 에너지만 쏴서 내장지방을 자멸사시키는 것
물리학과 공학의 영역에서 답을 찾는 방향임
5.1. 1064nm 레이저: 피부는 안 태우고 지방층까지 파고드는 빛
비침습 지방 제거 기술 하면 가장 먼저 떠오르는 게 냉동지방분해술(Cryolipolysis) 임
쿨스컬프 같은 시술이 이 방식인데 기기를 피부에 붙여서 지방 세포를 얼려서 죽이는 방식임
근데 이 기술에는 명확한 한계가 있음
기기를 피부에 부착할 수 있는 부위의 피하지방에만 적용 가능함
기기가 닿지 않는 복강 깊숙한 내장지방엔 쓸 수가 없음
이 한계를 돌파하기 위해 나온 게 고온 광열 방식 레이저 임
핵심 파장이 1064nm 다이오드 레이저 인데
이 파장이 왜 특별하냐
빛이 피부를 통과할 때 에너지 손실이 일어나는 이유가 두 가지임
첫째, 피부 속 수분이 빛을 흡수함
둘째, 표피의 멜라닌 색소가 빛을 흡수함
이 두 가지에 많이 흡수되는 파장의 레이저를 쏘면
표피와 진피에서 에너지가 다 소모되고 피부에 화상이 생김
깊은 곳까지 에너지가 닿지 않음
1064nm 파장은 이 두 가지에 대한 흡수율이 둘 다 낮음
수분도 별로 안 흡수하고 멜라닌도 별로 안 흡수함
그래서 표피와 진피를 사실상 그냥 통과해서 그 아래 지방층까지 에너지가 전달됨
동시에 피부 표면은 냉각 시스템으로 보호하면서 시술함
피부는 차갑게 식히고, 그 아래 지방층은 레이저로 가열하는 구조임
지방층 안에서 어떤 일이 일어나냐
레이저 에너지가 집중되면서 지방 조직 내부 온도가 42°C에서 최대 47°C까지 올라감
이 온도가 20분 이상 유지되면 지방 세포에 두 가지 일이 동시에 일어남
첫째, 지질이 분해되어 혈중으로 방출됨
지방 세포 안에 있는 트리글리세라이드는 고체에 가까운 형태로 저장돼 있음
온도가 올라가면 이게 녹으면서 유리지방산과 글리세롤로 분해됨
이 분해산물이 세포막을 통해 혈중으로 흘러나와 에너지원으로 소비됨
둘째, 지방 세포 자체가 자멸사함
43°C 이상의 열은 지방 세포에게 치명적인 스트레스임
세포막의 물리적 구조가 손상되고
세포 안에서 소포체 스트레스가 일어나면서
열에 극도로 민감한 성숙 지방 세포가 자멸사로 사라짐
중요한 건 혈관은 이 온도에서 살아남는다는 거임
혈관 세포는 지방 세포보다 열에 강해서 보존되고
지방 세포만 선택적으로 파괴되는 효과가 나타남
자멸사된 지방 세포와 잔해들은
이후 수 주에 걸쳐 림프계를 통해 대식세포가 탐식해서 영구적으로 제거됨
임상 연구에서 1회 시술 후 12주 뒤 복부 지방 두께가 약 8.5~15% 감소했음
시술 한 번으로 이 정도면 상당한 수준임
5.2. HIFEM: 근육을 강제로 수축시켜서 내장지방을 간접 폭격하기
이 기술은 방향이 완전히 다름레이저는 직접 열을 지방에 가하는 방식이었는데HIFEM은 지방을 직접 건드리지 않음대신 근육을 극한까지 몰아붙여서 내장지방이 스스로 분해되도록 몸을 강제하는 방식임HIFEM이 뭔지 먼저 설명하면High-Intensity Focused Electromagnetic, 고강도 집속 전자기장임원래 근력 강화 목적으로 의료 미용 시장에 나온 기기임배에 기기를 붙이면 전자기파가 나오면서 복부 근육이 수축함근데 이 기기를 쓰다 보니 의도치 않은 효과가 발견됐음내장지방이 줄어드는 거임근육을 강화하려고 쓴 기기인데 왜 내장지방이 사라지냐이 메커니즘을 파고들었더니 예상을 뛰어넘는 과정이 밝혀졌음작동 원리를 단계별로 보면 이럼1단계: 뇌의 통제 범위를 넘는 근수축 유발HIFEM의 전자기파는 교류 자기장을 형성해서 복부 골격근 안의 운동 뉴런을 직접 탈분극시킴운동 뉴런이 탈분극되면 근육이 수축함일반적인 운동을 할 때 뇌는 근육을 최대 60~70% 정도 동원함안전을 위해 뇌가 알아서 제한을 거는 거임근데 HIFEM은 이 제한을 우회해서 100% 강도의 수축을 강제로 유발함이걸 초극대 근수축(Supramaximal contractions) 이라고 함30분 동안 수만 번 이 수축이 반복됨인간이 의지로는 절대 낼 수 없는 강도의 수축이 기계적으로 강제되는 거임2단계: 근육 안에 에너지 위기가 발생함이 극단적인 수축이 반복되면서 근육 안의 ATP가 폭발적으로 소모됨ATP는 세포의 에너지 화폐임이게 바닥나기 시작하면 근육 조직 안에서 극심한 에너지 부족 상태가 만들어짐3단계: 몸이 비상 모드 돌입에너지 위기를 감지한 몸은 긴급하게 에너지를 조달해야 함이때 에피네프린을 포함한 카테콜아민 호르몬이 대량으로 분비됨카테콜아민은 지방 세포에 "지금 당장 지질 분해해라" 는 강력한 신호를 보냄이 신호를 받은 피하지방과 내장지방 세포들이 저장된 트리글리세라이드를 유리지방산으로 분해하기 시작함4단계: 유리지방산이 범람하면서 지질 독성 발생지방 세포들이 너무 빠르게 너무 많은 유리지방산을 방출함근육이 이 지방산을 소비하는 속도보다 방출 속도가 훨씬 빠름결과적으로 지방 세포 주변에 유리지방산이 과도하게 쌓임이 상태를 지질 독성(Lipotoxicity) 이라고 함5단계: 지질 독성이 지방 세포 자멸사를 유도함유리지방산이 과도하게 차오르면 지방 세포 안에서 소포체 스트레스(ER stress) 가 폭발적으로 증가함소포체는 세포 안에서 단백질을 합성하고 처리하는 기관인데지질 독성 환경에서는 이 기관이 정상 기능을 잃고 스트레스 반응이 한계를 넘음이 한계를 초과한 소포체 스트레스가 자멸사 신호를 켜버림주변의 내장지방 세포들이 연쇄적으로 자멸사에 들어감임상 데이터를 보면 효과가 상당함22명 대상으로 복부에 주 2회씩 총 8회 HIFEM 시술 후CT로 내장지방을 측정했더니내장지방 면적이 평균 110.6 cm²에서 93.9 cm²로 줄었음복강 전반에 걸쳐 내장지방이 감소한 게 확인됐음이 기술의 의미가 뭐냐외과 수술 도구도 없고, 약물도 없고, 나노입자도 없음기기를 피부 위에 붙이고 전자기파를 쏘는 게 전부임그런데 근육 → 에너지 위기 → 카테콜아민 분비 → 지방 분해 → 지질 독성 → 내장지방 자멸사라는 연쇄 반응이 일어나서 복강 깊숙한 내장지방이 사라짐직접 건드릴 수 없는 내장지방을 몸의 대사 경로를 강제로 교란해서 간접적으로 분해시키는 방식임한 줄 요약하면: 레이저는 피부를 통과해서 직접 지방층에 열을 가해 자멸사를 유도하고, HIFEM은 근육을 극한까지 수축시켜 에너지 위기를 만들어 몸이 스스로 내장지방을 분해하게 강제하는 방식임그렇다면 이렇게 다양한 기술이 나오고 있는데도 왜 실제 임상으로 넘어오는 게 쉽지 않을까?
지금까지 나온 기술들을 정리하면나노 약물, 광역학 치료, 레이저, HIFEM까지내장지방을 공략하는 전략이 다양하게 쏟아지고 있음근데 이 모든 기술이 인체에 적용되기 전에 반드시 거쳐야 하는 단계가 있음전임상 실험, 즉 동물 실험임동물에서 효과와 안전성이 확인돼야 사람 대상 임상시험으로 넘어갈 수 있음
여기서 내장지방 치료 연구 전체가 공유하는 결정적인 병목이 있음마우스는 사람이 아님마우스 실험의 한계가 뭐냐마우스 모델은 기초 메커니즘을 이해하는 데 엄청난 역할을 해왔음FAT-ATTAC 같은 모델도 마우스에서 나온 연구임근데 문제는 마우스와 인간 사이에 생물학적 차이가 너무 많다는 거임대표적으로지방 조직의 구조와 분포 방식이 다름호르몬 분비 패턴이 다름면역 반응 방식이 다름인슐린 저항성이 발생하는 메커니즘도 세부적으로 다름
그래서 마우스에서 완벽하게 효과가 나온 약물이인체 임상에서 효과가 없거나 예상치 못한 독성이 나타나는 경우가 반복됨신약 개발에서 임상 1상이나 2상에서 실패하는 약물의 상당수가동물 실험에서는 성공했지만 인체에서 결과가 달랐던 케이스임이게 단순히 돈과 시간의 문제가 아님마우스 실험 과정에서 수많은 동물이 희생되는 윤리적 문제도 있고무엇보다 인체에서의 결과를 예측하지 못한다면임상 설계 자체가 흔들리는 근본적인 문제임
이 한계를 돌파하기 위해 UNIST 연구진이 개발하고 있는 게미세생리시스템(MPS, Microphysiological Systems) 임쉽게 말하면 칩 위에 인간 지방 조직을 만드는 기술임
장기 칩이 뭔지부터 설명하면Organ-on-a-chip이라는 개념임손가락 한 마디 크기 정도의 칩 위에인간 세포를 배양해서 실제 장기와 유사하게 작동하도록 만든 시스템임단순히 페트리 접시에 세포를 키우는 것과 차원이 다름페트리 접시는 2D 평면에서 세포가 자라는 환경이라 실제 체내 환경과 많이 다름장기 칩은 3D 구조로 세포를 배양하고혈류와 유사한 액체 흐름까지 만들어서 체내 환경을 최대한 모사함
UNIST 연구진이 만든 건 지방 조직 칩임구체적으로 어떻게 만들었냐칩의 재료실리콘이나 PDMS라는 유연한 고분자 소재로 미세유체 칩을 제작함PDMS는 투명하고 세포 독성이 없으며 정밀한 미세구조를 만들기 쉬운 소재임이 칩 위에 머리카락 굵기보다 훨씬 얇은 미세 채널들이 새겨져 있음
칩 위에 올리는 세포두 종류의 인간 유래 세포를 씀지방전구세포: 지방 세포로 분화할 수 있는 전구 세포대식세포: 면역 세포이 두 세포를 단순히 섞어서 키우는 게 아님3D 스페로이드 형태로 공동 배양함스페로이드는 세포들이 3차원으로 뭉쳐서 실제 조직과 유사한 덩어리를 형성한 상태임실제 지방 조직 안에서 지방 세포와 대식세포가 함께 존재하면서 상호작용하는 것과 유사한 환경을 만드는 거임
혈류를 흉내 내는 미세유체 채널칩 안의 미세 채널로 포도당, 인슐린, 나노 약물 같은 물질을 정밀하게 흘려보냄실제 혈류가 조직에 영양소와 약물을 공급하는 것과 유사한 환경을 재현하는 거임농도도 조절하고 흐름 속도도 조절할 수 있음
이 시스템으로 뭘 볼 수 있냐첫째, 인슐린 저항성이 생기는 과정을 실시간으로 관찰함포도당과 인슐린 농도를 조절하면서 칩 위의 지방 세포가 인슐린 저항성을 획득하는 과정을 추적할 수 있음아디포넥틴이나 IL-6 같은 사이토카인 분비가 어떻게 변하는지도 실시간으로 측정 가능함이게 중요한 이유는 인슐린 저항성이 어떤 분자적 과정을 통해 생기는지를 인간 세포에서 직접 볼 수 있기 때문임마우스 데이터가 아닌 인간 세포 데이터임둘째, 나노 약물이 실제로어떻게 작동하는지 추적함PCL-DSF나 MSNs-ATS 같은 나노 약물을 칩에 흘려보내면약물이 어떤 세포에 얼마나 흡수되는지자멸사가 언제 어느 세포에서 시작되는지얼마나 선택적으로 작동하는지를동물 없이 분자 수준에서 실시간으로 확인할 수 있음셋째, 약물 병용 효과를 미리 검증함CBL-514와 GLP-1 같은 병용 요법을 동물 실험 전에 칩에서 먼저 테스트할 수 있음어떤 농도 조합이 가장 효과적인지, 독성은 없는지를 사전에 확인하는 거임
이게 왜 중요하냐신약이 개발되어 실제 환자한테 쓰이기까지 걸리는 시간이 보통 10년 이상임그 과정의 상당 부분이 동물 실험이고동물에서 인체로 넘어가는 과정에서 예측 실패로 임상이 중단되는 경우가 많음MPS 기술이 고도화되면 이 과정이 바뀔 수 있음동물 실험과 인체 임상 사이에 인간 세포 기반의 검증 단계가 추가되는 거임마우스에서 효과가 나왔어도 인간 지방 조직 칩에서 같은 결과가 안 나오면 임상 진입을 재검토할 수 있고반대로 마우스에서 약간 애매했어도 인간 세포 칩에서 강한 효과가 나오면 임상 설계에 자신감을 가질 수 있음즉 임상 실패율을 낮추고 개발 기간을 단축시키는 인프라가 되는 거임UNIST가 이 연구를 주도하고 있다는 것 자체도 주목할 만함내장지방 MPS 연구는 나노 의학, 바이오공학, 대사 의학이 동시에 교차하는 영역인데이 분야에서 세계적 수준의 연구가 한국에서 나오고 있는 거임
한 줄 요약하면: 마우스 실험의 한계를 극복하기 위해 칩 위에 인간 지방 조직을 3D로 재현한 뒤, 약물과 혈류 환경을 정밀하게 시뮬레이션해서 동물 없이 인간 수준의 반응을 예측하는 기술임
결론&정리 : 내장지방 전쟁, 지금 어디까지 왔나
지금까지 나온 기술들을 한번 다 펼쳐놓고 보면 뭔가 큰 흐름이 보임
처음엔 단순했음살을 빼려면 덜 먹으면 됨그래서 식욕을 억제하는 약을 만들었고위고비, 마운자로가 나왔고실제로 체중을 크게 줄이는 데 성공했음
근데 문제가 생겼음약을 끊으면 다시 찜지방 세포의 크기는 줄었지만 개수는 그대로였으니까몸은 기회만 생기면 원래 상태로 돌아가려고 했음
그래서 질문이 바뀌기 시작함"어떻게 하면 더 많이 빼냐"가 아니라 "왜 다시 찌냐"를 파고들기 시작한 거임
여기서 내장지방이 핵심으로 떠올랐음내장지방은 그냥 배가 나온 미용의 문제가 아니라간으로 직접 연결된 염증 공장이고인슐린 저항성과 대사 증후군의 진짜 원인이었음근데 이걸 직접 없앨 방법이 없었음바늘을 배 안에 넣으면 장기가 뚫리고레이저를 쏘면 피부에 화상이 생기고약을 넣으면 엉뚱한 곳으로 퍼졌음
과학자들이 이 벽을 넘기 위해 다섯 방향에서 동시에 달려들었음
첫 번째 방향: 우회CBL-514로 피하지방 창고를 없애버리고GLP-1 약으로 전신 지방 분해 신호를 때리면몸이 갈 곳이 없어진 에너지를 내장지방에서 끌어다 쓰기 시작함직접 못 가면 몸이 스스로 태우게 만드는 거임결과가 내장지방 -367% 추가 감소였음
두 번째 방향: 정밀 침투나노입자에 GPS를 달아서 내장지방만 찾아가게 만들었음P-G3는 전하 차이로 내장지방 ECM에 달라붙고PCL-DSF는 지방 전구세포만 골라서 자멸사시키고MSNs-ATS는 프로히비틴 수용체를 찾아가서 지방을 갈색지방으로 바꿔버림세 번째 방향: 빛으로 태우기AIEgens 감광제는 지질 방울 안에 농축된 뒤산소 없이도 자유 라디칼을 만들어서 지방 세포를 내부에서 터뜨림동물 실험에서 내장지방 65% 이상 감소복강경 광섬유와 결합하면 배 안에서 레이저로 직접 태우는 것도 가능함네 번째 방향: 죽이는 방식이 중요하다는 걸 증명함FAT-ATTAC 모델이 밝혀낸 것은지방 세포를 없애는 것 자체보다 어떻게 없애냐가 전부라는 거임괴사로 터지면 M1 대식세포가 달려와서 염증 폭탄이 터짐자멸사로 깔끔하게 사라지면 M2 대식세포가 와서 조직을 수복함치료의 방향이 자멸사여야 하는 이유를 분자 수준에서 증명한 거임다섯 번째 방향: 아무것도 안 넣고 외부에서 때리기1064nm 레이저는 피부를 통과해서 지방층을 42~47°C로 가열해 자멸사 유도HIFEM은 근육을 뇌의 통제 범위 밖으로 수축시켜서에너지 위기 → 카테콜아민 분비 → 지질 독성 → 내장지방 자멸사로 이어지는순수한 대사적 강제로 복강 깊숙한 지방을 분해함약도 나노입자도 없이 기기만으로 내장지방 14.3% 감소그리고 이 모든 기술이 인체에 제대로 적용되려면마우스와 사람의 차이를 넘어야 한다는 문제가 남았음UNIST가 이걸 공략하고 있음칩 위에 인간 지방 조직을 3D로 만들어서동물 실험 없이 인간 수준의 반응을 사전에 검증하는 인프라를 구축 중임이 흐름 전체를 하나의 문장으로 압축하면 이럼비만치료 연구는 "얼마나 빼냐"의 시대에서 "어디서 어떻게 빼냐"의 시대로 넘어가고 있음내장지방 때문에 생기는 당뇨, 지방간, 대사 증후군이지금과 완전히 다른 방식으로 다뤄지는 세상이 열릴 수 있다는 거지비만 치료 역사에서 가장 큰 전환점이지금 막 시작되고 있음
출처: 에펨코리아

[0]

[0]
[0]

[0]
[0]

[0]
[0]

[0]

[0]

[0]

[0]

[0]
[0]

[0]

[0]

[0]

[0]

[0]
[0]

[0]
